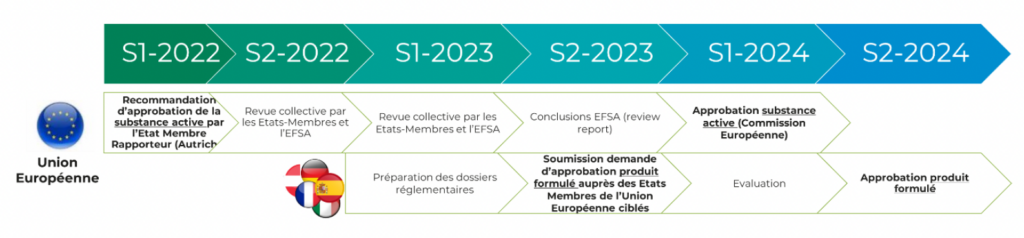
Calendrier réglementaire de l’application biocontrôle en Europe conforme aux prévisions
AMOEBA : Calendrier réglementaire de l’application biocontrôle en Europe conforme aux prévisions
Chassieu (France), le 13 juillet 2023– 08h30 – AMOÉBA (FR0011051598 – ALMIB), biotech industrielle en pré-commercialisation* spécialisée dans le traitement du risque microbiologique, développant un agent de biocontrôle pour le traitement des plantes en agriculture et un biocide biologique pour le traitement de l’eau industrielle, confirme que le calendrier réglementaire de demande d’approbation de la substance active de biocontrôle est conforme aux prévisions de la Société.
L’EFSA, l’Agence Européenne de Sécurité des Aliments, mentionne sur son site internet une date limite pour l’évaluation des risques (Risk Assessment Deadline) au 19 juillet 2023. Cette date ayant été assignée par défaut lors du démarrage de la revue collective du dossier en décembre 2022, elle ne prend pas en compte un éventuel délai pris par les autorités.
La Société a anticipé ce décalage possible dans ses prévisions : le calendrier réglementaire pour l’application biocontrôle en Europe, tel que publié dans le Document d’Enregistrement Universel 2022 déposé le 18 avril 2023 sous le numéro D23-0296 auprès de l’AMF et disponible sur le site internet de la Société, est toujours valide et rappelé ci-dessous :
- La phase d’évaluation du risque se terminant par le rapport scientifique (peer-review report) de l’EFSA contenant ses conclusions devrait être finalisée au second semestre 2023.
- La phase de gestion du risque se terminant par la publication du règlement d’exécution portant décision de la Commission Européenne au Journal officiel de l’UE devrait être finalisée premier semestre 2024.
Les demandes d’approbations pour les produits formulés pouvant être soumises avant l’approbation définitive de la substance active, le calendrier prévisionnel pour les produits formulés est également conforme aux prévisions :