Résultats significatifs de l’étude menée sur 30 patients par l’Institut d’Expertise Clinique
Chassieu (France), le 10 juin 2024, – 17h45 – AMOÉBA (FR0011051598 – ALMIB), greentech industrielle spécialisée dans le traitement du risque microbiologique, développant un agent de biocontrôle pour la protection des plantes en agriculture et une gamme d’ingrédients cosmétiques, annonce avoir obtenu les résultats de l’étude clinique confirmant l’intérêt de l’usage de son ingrédient en cosmétique pour le soin de la peau.
En octobre 2023, pour donner suite à des tests de son ingrédient réalisés sur peau artificielle ayant démontré d’excellents résultats, Amoéba a annoncé le lancement d’une nouvelle application majeure dans le domaine de la cosmétique (cf. Communiqué de presse du 16 octobre 2023).
Une première étude clinique a été réalisée par l’Institut d’Expertise Clinique portant sur 30 volontaires en hémi-visage (n=60) en mars et avril 2024. Cette étude, confirme l’intérêt de l’usage de notre ingrédient en cosmétique pour le soin de la peau avec des résultats mesurés « statistiquement significatifs » justifiant les allégations suivantes :
- « amélioration de l’épaisseur du derme »
- « effet réparateur sur le derme superficiel »
- « amélioration de la densité de la peau »
- « amélioration de la texture du derme »
Amoéba a également obtenu l’inscription de cet ingrédient actif sur la liste de l’INCI (nomenclature internationale pour les ingrédients cosmétiques), ouvrant ainsi la voie, sans autre autorisation nécessaire, à la commercialisation et à la recherche de partenariats commerciaux.
Le marché du soin de la peau est estimé à 200 milliards de dollars en 2023, avec une croissance annuelle attendue de de 6% par an jusqu’en 2030 (source Mc Kinsey – The beauty market in 2023).
Le management d’Amoéba aura l’occasion de présenter sa stratégie le 12 juin à Paris lors de la Conférence annuelle Mid & Small Caps Portzamparc BNP Paribas Group. La mise en ligne de la présentation utilisée pour cet évènement sera effective mardi 11 juin à 19h au plus tard sur le site internet de la société.
ASSEMBLEE GENERALE ORDINAIRE ET EXTRAORDINAIRE DU 27 MAI 2021
MODALITES DE MISE À DISPOSITION DES DOCUMENTS PREPARATOIRES
Les actionnaires de la société sont invités à participer à l’assemblée générale ordinaire et extraordinaire qui se tiendra le :
Jeudi 27 mai 2021, à 9 heures,
Au siège social de la société – 38 Avenue des frères Montgolfier – 69680 CHASSIEU
L’avis de réunion comportant l’ordre du jour et les projets de résolutions a été publié au BALO du 21 avril 2021 et l’avis de convocation au BALO du 10 mai 2021.
Les documents prévus par l’article R.225-83 du code de commerce sont tenus à la disposition des actionnaires à compter de la convocation de l’assemblée, conformément aux dispositions réglementaires applicables :
- tout actionnaire nominatif peut, jusqu’au cinquième jour inclusivement avant l’assemblée, demander à la société de lui envoyer ces documents. Pour les titulaires d’actions au porteur, l’exercice de ce droit est subordonné à la fourniture d’une attestation de participation dans les comptes de titres au porteur tenus par l’intermédiaire habilité ;
- tout actionnaire peut en prendre connaissance au siège de la société pendant un délai de 15 jours précédant la date de l’assemblée.Pour information, le vote électronique via la plateforme de vote sécurisée VOTACCESS pour l’Assemblée Générale du jeudi 27 mai 2021 sera ouvert du 10 mai 2021 jusqu’au mercredi 26 mai 2021 à 15h00 (heure de Paris). Les actionnaires souhaitant utiliser cette plateforme peuvent consulter les modalités d’accès sur l’avis de convocation et sur le site de la société (ici)
Le résultat des votes des résolutions sera affiché sur le site Internet de la Société.
Avertissement
Dans le contexte d’épidémie de coronavirus (COVID-19), les modalités de tenue de l’Assemblée Générale pourraient évoluer en fonction des impératifs sanitaires et/ou légaux.
Les actionnaires sont, en conséquence, invités à consulter régulièrement la rubrique dédiée à l’Assemblée Générale sur le site de la Société (https://amoeba-nature.com/investisseur/assemblee- generale).
Précisions sur le calendrier des différents dossiers réglementaires
Chassieu (France), le 06 avril, 2021 – 17h45 – AMOÉBA (FR0011051598 – ALMIB), producteur d’un biocide biologique capable d’éliminer le risque bactérien dans l’eau et les plaies humaines, et d’un produit de biocontrôle pour la protection des plantes, encore en phase de développement, a déposé ce jour la demande d’approbation de la substance active biocide, l’amibe vivante Willaertia magna C2c Maky, et des produits biocides la contenant, auprès del’Agence américaine de Protection de l’Environnement, l’U.S. EPA (U.S. Environmental Protection Agency).
Amoéba rappelle qu’en août 2019, elle avait décidé de retirer volontairement son dossier de demande d’approbation de la substance active biocide, l’amibe vivante Willaertia magna C2c Maky, et des produit biocides la contenant, pour déposer ultérieurement une nouvelle demande d’approbation.
Lors d’une réunion de « pré-soumission », en novembre 2019, entre Amoéba et l’U.S. EPA, des demandes de précisions sur certains éléments scientifiques qui ont conduit au retrait du dossier ont été évoquées ainsi que la manière dont Amoéba envisageait d’y répondre.
Amoéba a ainsi pu soumettre ce jour une nouvelle demande, avec les études complémentaires requises par l’U.S. EPA.
Une fois que les homologations de la substance active et du produit biocide seront obtenues, envisagées mi- 2022 sous réserve d’approbation par l’US EPA, un enregistrement (notification et paiement de taxes) sera nécessaire au niveau des États nécessitant un délai d’environ deux mois (exception faite de la Californie qui requière une évaluation du dossier complète d’environ 12 mois). Une fois l’enregistrement obtenu au niveau local, la commercialisation pourra être possible dans l’Etat.
Amoéba envisage ainsi une commercialisation de son produit biocide aux Etats-Unis à partir du second semestre 2022, sous réserve d’une décision positive de l’U.S. EPA.
Précisions sur le calendrier des autres dossiers réglementaires biocides et phytosanitaires
Amoéba informe également sur le calendrier réglementaire des différents dossiers réglementaires :
- Application biocide (substance active biocide, Willaertia magna C2c Maky vivante) :
- Europe : la demande d’approbation de la substance active, soumise en 2019 (voir Communiqué de Presse du 12 aout 2019), est en cours d’évaluation par l’autorité maltaise. Amoéba considère que le rapport d’évaluation de l’autorité pourrait être disponible mi-2021.
- Canada : le dossier de demande d’homologation de la substance active et des produits biocides la contenant, soumis en 2019 (voir Communiqué de Presse du 1er février 2019) est en cours d’évaluation. L’extension de la durée d’évaluation (initialement estimée à 24 mois) est due à une demande d’informations complémentaires de l’agence canadienne à laquelle la société a répondu. Amoéba estime que la décision de l’agence canadienne pourrait intervenir avant la fin de l’année 2021.
- Application phytosanitaire (substance active de biocontrôle, Lysat de Willaertia magna C2c Maky) :
- Europe : la demande d’approbation de la substance active, soumise en 2020 (voir Communiqué de Presse du 29 mai 2020), est en cours d’évaluation par l’autorité autrichienne. Amoéba considère que le rapport d’évaluation de l’autorité pourrait être disponible fin 2021.
- Etats-Unis : le dossier de demande d’homologation de la substance active et des produits la contenant, soumis en 2020 (voir Communiqué de Presse du 1er octobre 2020) est en cours d’évaluation. La décision de l’agence américaine devrait intervenir courant 2022.
- Brésil : un permis d’expérimentation a été obtenu en février 2021, permettant à la Société d’initier des essais au champ sur le soja, le caféier et le bananier. De tels essais sur le territoire brésilien sont requis pour un dossier de demande d’approbation.Le détail des procédures est disponible dans le Document d’Enregistrement Universel (URD) déposé auprès de l’Autorité des Marchés Financiers le 30 avril 2020 sous le numéro D20-0416, en particulier à la sous-section 5.4.3 « Procédures d’enregistrement des produits ». L’URD est disponible sur le site internet de la société et sa mise à jour, incluant les informations ci-dessus, sera publiée courant avril 2021.
Chassieu (France), le 6 avril , 2021 – 8h30 – AMOÉBA (FR0011051598 – ALMIB), producteur d’un biocide biologique capable d’éliminer le risque bactérien dans l’eau et les plaies humaines, et d’un produit de biocontrôle pour la protection des plantes, encore en phase de développement, annonce, dans le cadre du développement de sa substance active biofongicide, le lysat de l’amibe Willaertia magna C2c Maky, qu’elle étend ses collaborations avec ses partenaires (PHILAGRO et STÄHLER) etd’autres acteurs majeurs du secteur de la protection des plantes (BASF – BAYER –– EVERGREEN GARDEN CARE – GOWAN – KWIZDA) .
Poursuite des expérimentations avec les partenaires
PHILAGRO (France) et STÄHLER (Suisse), les sociétés partenaires avec lesquelles AMOÉBA a déjà signé des « term sheets » devant conduire à la signature d’un accord de distribution sur vigne (Cf. communiqués de presse des 9 et 18 décembre 2020), vont poursuivre leurs expérimentations sur celle-ci mais également sur d’autres cultures.
L’application de biocontrôle testée sur d’autres cultures et zones géographiques
D’autres acteurs de l’agrochimie, dont certains ont déjà effectué des tests en 2020, ont décidé de prendre part à cette nouvelle campagne d’essais au champ. Ainsi, BASF – BAYER –– EVERGREEN GARDEN CARE – GOWAN – KWIZDA testeront la substance active d’AMOEBA dans différents pays et sur un large spectre de cultures (dont la vigne, les céréales et les cultures maraichères).
Avec les essais réalisés en propre par AMOÉBA, plus de 200 essais au total sont programmés dans le monde (Europe, Amériques, Asie) en 2021. Cette très large campagne permettra d’approfondir les connaissances sur la substance active, de comparer plusieurs formulations, d’élargir la connaissance du spectre d’activité et de générer, en Europe, des résultats pour alimenter les futurs dossiers de demande de mise en marché des produits formulés de biocontrôle.
« Cette nouvelle campagne d’essais au champ, à laquelle de nouveaux acteurs de l’agrochimie ont pris part, démontre la nécessité d’agir vite pour trouver des solutions alternatives au tout chimique. L’agriculture actuelle, face à de plus en plus de restrictions d’utilisation des produits phytosanitaires, doit relever de nombreux défis environnementaux pour répondre aux attentes du marché et des consommateurs. Fort de ces 200 essais programmés dont plus de 70 en propre, AMOEBA et sespartenaires sont décidés à accompagner l’ensemble des acteurs du monde agricole pour mener à bien une véritable transition agroécologique », déclare Fabrice PLASSON, Président Directeur Général d’Amoéba.
Chassieu (France), le 26 mars 2021-8h15- AMOEBA (FR0011051598 – ALMIB), producteur d’un biocide biologique capable d’éliminer le risque bactérien dans l’eau et les plaies humaines, et d’un produit de biocontrôle pour la protection des plantes, encore en phase de développement, annonce aujourd’hui ses résultats annuels 2020.
Le Conseil d’Administration, qui s’est réuni le 25 mars 2021, a arrêté les comptes sociaux et consolidés du Groupe Amoéba pour l’exercice clos le 31 décembre 2020.
Les Commissaires aux Comptes ont effectué leurs travaux d’audit et n’ont pas relevé d’anomalie significative de nature à remettre en cause la conformité de ces derniers. Les rapports de certification sont en cours d’émission.
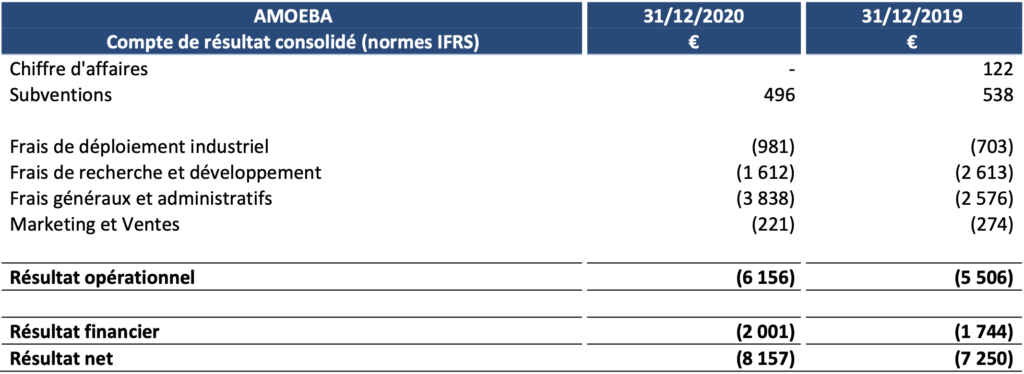
Des résultats 2020 impactés par le coût des études règlementaires
Au 31 décembre 2020, le résultat opérationnel d’Amoéba s’établit à -6 156 K€ contre -5 506 K€ au 31 décembre 2019.
- La société n’a réalisé aucun chiffre d’affaires au cours de l’exercice 2020.
- Les subventions restent stables par rapport à 2019. Elles sont constituées du Crédit Impôt Recherche et reflètent les efforts faits par l’entreprise en matière de recherche et développement sur son application biocontrôle au cours de l’année 2020.
- Les frais de déploiement industriel sont en légère hausse par rapport à l’année précédente.
- Les dépenses de Recherche et Développement s’établissent à 1 612 K€ en baisse par rapport à 2019 (2 634 K€). Cette baisse est due à une dépréciation exceptionnelle des frais de développement pour 933 K€ passée en juin 2019 suite au retrait de la demande d’autorisation de mise sur le marché (AMM) aux Etats Unis et le décalage consécutif des opérations de production (cf. communiqué de presse du 19 août 2019).
- Les frais de marketing et ventes (221 K€) sont en diminution (274 K€en2019).
- Les frais généraux et administratifs s’établissent à 3 838 K€, en hausse de 1 262 K€ par rapport à l’année précédente. Cet écart est dû aux coût des études règlementaires, à l’augmentation des honoraires relatifs aux opérations financières et à la gestion des brevets.
- Le résultat financier comprend principalement des charges d’intérêts liés aux emprunts bancaires (1 546 K€), à l’opération OCAPI (359 K€) et aux pertes de change.
Le résultat net s’établit ainsi à -8 157 K€ contre -7 250 K€ au 31 décembre 2019.
Au 31 décembre 2020, les capitaux propres de la société s’élèvent à 2 M€ contre 4,2 M€ au31 décembre 2019.
L’endettement financier de la société s’élève à 8,6 M€ et est principalement constitué du prêt BEI (5 M€) et des intérêts capitalisés (2,9 M€), ainsi que des dettes liées aux obligations locatives (0,7 M€).
La trésorerie de la Société au 31 décembre 2020 s’élève à 4 975 K€ contre 4 761 K€ au 31 décembre 2019.
Une année principalement marquée par l’accélération du développement de l’application biocontrôle pour la protection des plantes et la poursuite des dossiers règlementaires de commercialisation des applications biocontrôle et biocide
Au cours de l’année 2020, Amoéba s’est concentrée sur les axes principaux suivants :
1. Accélérationdudéveloppementdel’applicationbiocontrôlepourlapréventiondesmaladiesdes plantes notamment au travers de partenariats de recherche avec des groupes industriels majeurs
- Au cours de l’année 2020, la Société a annoncé la signature de 8 contrats de transfert de matériel (MTA) avec les sociétés De Sangosse, Certis Europe, Stähler Suisse, BASF, Philagro France & Nichino Europe, Evergreen Garden Care, Syngenta et Bayer.
Ces accords avaient pour objet de mettre à la disposition de ces sociétés différentes formulations de produits expérimentaux contenant la substance active d’Amoéba : le lysat d’amibe Willaertia magna C2c Maky. En contrepartie, les huit groupes agrochimistes ont financé et procédé à leurs propres essais en plein champ, afin d’évaluer les performances de ces produits à prévenir les maladies sur différentes cultures. - La Société a confirmé l’efficacité de son lysat d’amibe Willaertia Magna C2c Maky contre le mildiou de la vigne lors de la seconde campagne de tests aux champs (cf communiqué de presse du 27 juillet 2020).
Elle a, par ailleurs, annoncé les premiers résultats d’efficacité de sa solution de biocontrôle sur plusieurs maladies majeures du blé dans le cadre de ses essais aux champs (cf communiqué de presse du 22 juillet 2020). - Le 11 août 2020, la Société a annoncé la publication d’un premier article scientifique, évalué par des pairs, sur son application biocontrôle (https://www.mdpi.com/2223- 7747/9/8/1013/pdf) dans le numéro spécial « Natural Products for Plant Pest and Disease Control » de Plants.
- Le 1° Octobre 2020 la société a déposé une demande d’approbation de la substance active de biocontrôle, « lysat de Willaertia magna C2c Maky» et des produits la contenant, auprès de l’autorité américaine compétente , l’Agence de Protection de l’Environnement (EPA, Environmental Protection Agency).
- Le 7 décembre 2020, la Société a annoncé la signature d’un partenariat de recherche avec la société Gowan, un des principaux fournisseurs d’intrants agricoles (produits de protection des cultures, semences et engrais) aux Etats-Unis. Amoéba et le groupe Gowans’engagent ainsi dans une phase de recherche ciblée qui, si elle est concluante, pourrait favoriser le développement commercial des solutions de biocontrôle d’Amoéba aux Etats-Unis.
2. Poursuite des demandes d’autorisation de commercialisation (AMM) de l’application biocide
- En Europe : poursuite des discussions avec les autorités maltaises et leurs experts hollandais. Pour faire suite aux discussions et échanges réguliers avec les autorités et leurs experts, la Société estime pouvoir recevoir leur rapport d’évaluation mi- 2021.
- Aux Etats Unis : finalisation des études et rédactions des conclusions pour un dépôt du dossier Biocide USA prévu en avril 2021
A la demande des autorités américaines, des études complémentaires ont été effectuées en 2020. Ces études menées selon un protocole EPA – en complément des études OCDE déjà effectuées – ont démontré à nouveau l’innocuité de l’amibe Willaertia magna C2c Maky.Le dossier de demande d’autorisation de commercialisation sera déposé auprès de l’EPA en avril 2021.
3. Poursuite des travaux de recherche sur la connaissance de l’amibe Willaertia Magna C2c Maky
Au cours de l’année 2020, la société a publié plusieurs articles scientifiques relatifs à la connaissance de l’amibe Willaertia magna C2c maky :
- février 2020 : publication de résultats scientifiques réaffirmant l’effet direct de prédation etd’élimination des légionelles par l’amibe Willaertia magna C2c Maky(https://www.mdpi.com/2076-0817/9/2/105).
- mai 2020 : publication relative à l‘analyse du transcriptome et du protéome de l’amibe quand elle est cultivée à haut débit en bioréacteur (https://www.mdpi.com/2076-2607/8/5/771/pdf).
- juin 2020: publication apportant une preuve supplémentaire de l’inocuité de l’amibe dans lecadre de son utilisation en vue de lutter contre le risque de légionnelle(https://www.mdpi.com/2076-0817/9/6/447/pdf).
- novembre 2020: publication relative au développement et comportement de l’amibe produitede façon industrielle en bioréacteur (https://www.mdpi.com/2076-2607/8/11/1791/pdf).
4. Transfert des actions de la société du marché règlementé d’Euronext à Paris vers Euronext Growth
Lors de l’Assemblée Générale du 24 juin 2020, la Société a soumis au vote de ses actionnaires, qui l’ont approuvé, un projet de transfert de cotation de ses actions du marché réglementé d’Euronext Paris (compartiment C) vers le système multilatéral de négociation Euronext Growth Paris.
Ce transfert, qui a été réalisé le 14 septembre 2020, vise à permettre à Amoéba d’être cotée sur un marché plus adapté à sa taille et à sa capitalisation boursière, simplifier le fonctionnement de la Société et diminuer les coûts relatifs à sa cotation, tout en lui permettant de continuer à bénéficier des attraits des marchés financiers.
5. Sécurisation du financement de la société
- Renégociation du financement bancaire avec la Banque Européenne d’Investissement (BEI) et signature d’un contrat d’émission de Bons de Souscription d’Actions au profit de la BEI :
Le 31 mars 2020, la Société a signé un avenant au contrat de prêt conclu le 6 octobre 2017 avec la BEI en vue d’un projet d’émission de 200 000 Bons de Souscription d’Actions (BSA) au profit de la BEI.Aux termes de l’avenant, la BEI a accepté de supprimer définitivement l’engagement à la charge de la Société de maintenir le ratio initialement prévu entre le montant de ses capitaux propres et celui de ses actifs.
L’émission de ces BSA, a été approuvée par l’Assemblée Générale des actionnaires du 24 juin 2020 et décidée le 29 juillet 2020.L’avenant signé entre la BEI et Amoéba ne modifie pas l’exigibilité contractuelle du prêt BEI prévue en 2022. - Financements obligataires:
- Programme OCAPI 2020
L’Assemblée Générale Mixte des actionnaires du 13 mars 2020 a approuvé la mise en place d’un nouveau contrat d’émission d’obligations convertibles en actions avec programme d’intéressement (OCAPI) entre Amoéba et Nice & Green SA. Au 31 décembre 2020, 234 obligations sur 312 initialement prévues ont déjà été émises et totalement converties représentant la création de 2.783.957 actions nouvelles. - Nouveau programme OCAPI 2021-2022
Le 16 décembre 2020, la Société a signé un nouveau contrat de financement obligataire avec la société Nice & Green d’un montant de 23 M€. Conformément aux termes du contrat, l’Investisseur s’est engagé, sauf cas de défauts usuels, à souscrire des OCA par tranches émises trimestriellement selon l’échéancier suivant :- six (6) premières tranches composées de soixante (60) OCA ;
- une (1) tranche composée de quarante (40) OCA ; et
- une tranche optionnelle complémentaire de quatre-vingt (80) OCA.
- Cet échelonnement permet un financement régulier de la Société en limitant l’impact sur le cours de l’action.L’émission par Amoéba des OCA et l’émission éventuelle des actions nouvelles dont l’admission aux négociations sera demandée, est destinée à assurer la continuité d’exploitation jusqu’en septembre 20231 et notamment à financer :
- (i) les dépenses courantes liées à l’activité sur la période de financement dont les dépenses opérationnelles, les activités de recherche et développement sur l’application biocontrôle ainsi que le soutien des dossiers de demande d’autorisation de la substance active biocide et de la substance phytosanitaire en Europe et aux Etats Unis;
- (ii) le remboursement du Prêt BEI in fine prévu en novembre 2022 et des intérêts courus capitalisés jusqu’à l’échéance s’élevant à 11,8 M€.
- Programme OCAPI 2020
Impact de la crise sanitaire Covid 19 sur le développement de la Société
Dès le début du mois d’avril 2020, la production de la substance active de la Société a pu continuer dans des conditions normales d’exploitation. La crise sanitaire n’a pas eu d’impacts sur la préparation et le suivi des dossiers réglementaires en cours. La société a eu recours au mécanisme d’activité partielle de manière limitée et n’a pas sollicité de PGE.
La Société ne commercialise pas ses produits, et ne reconnait pas, à ce jour, de chiffre d’affaires significatif. La crise du Covid-19 a donc peu d’impact sur son compte de résultat.
Évolution récente et perspectives
Pour rappel, la Société ne commercialise à ce jour aucun produit et est en attente des autorisations de mise sur le marché selon les calendriers ci-dessous :
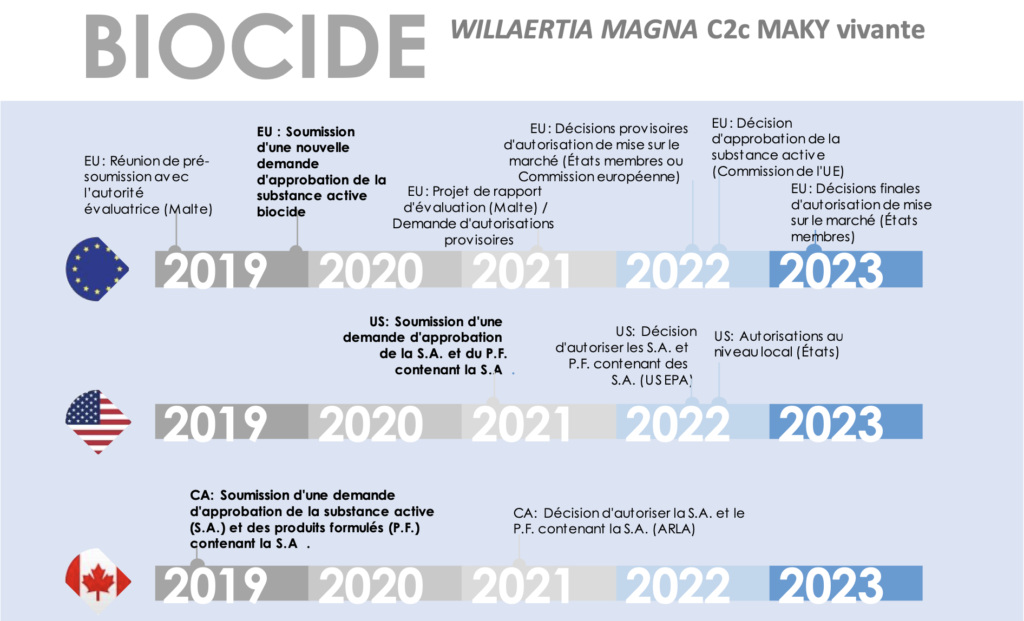
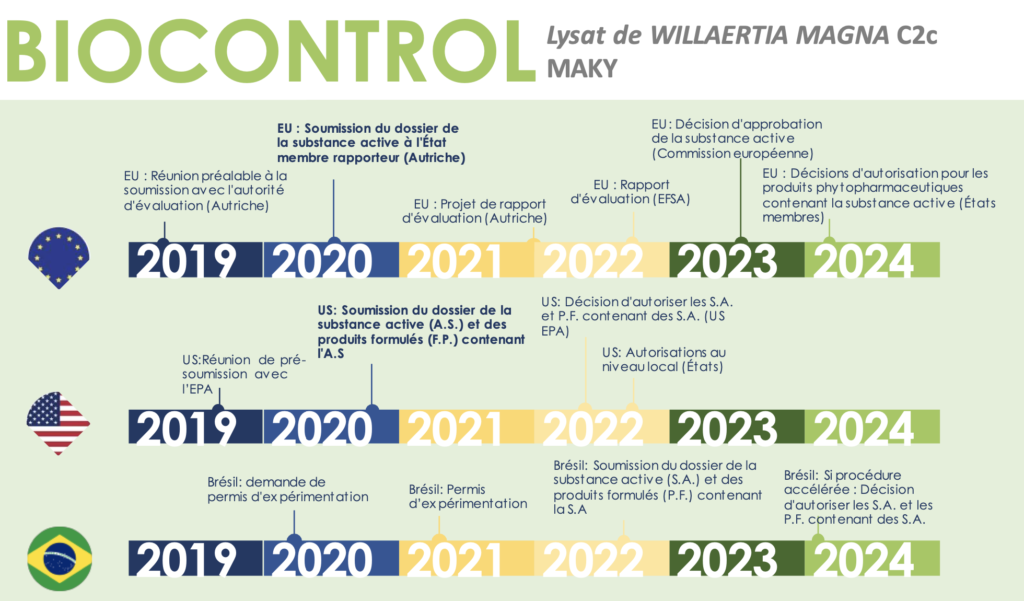
Les procédures de demande d’autorisation des applications biocide et biocontrôle, auprès des autorités réglementaires, sont détaillées dans le Document d’Enregistrement Universel déposé auprès de l’Autorité des Marchés Financiers le 30 avril 2020 sous le numéro D20-0416, en particulier à la sous- section 5.4.3 « Procédures d’enregistrement des produits ».
La société, en partenariat avec des entreprises agrochimiques de premier plan, se prépare à réaliser sur 2021 une troisième campagne de tests au champ de son produit de biocontrôle. Ces tests devraient essentiellement porter sur les maladies des céréales.
En parallèle des applications existantes (biocide et biocontrôle), Amoéba reçoit de nombreuses sollicitations pour intégrer sa solution dans de nouveaux champs d’exploitations. Une évaluation scientifique stricte de ces opportunités est menée en permanence par notre laboratoire et des laboratoires experts externes.
À la date d’arrêté des comptes, la Société dispose d’un fonds de roulement net suffisant pour faire face à ses obligations et à ses besoins de trésorerie sur les douze prochains mois, estimant pouvoir faire face à ses engagements pris jusqu’en septembre 2023. Les comptes clos au 31 décembre 2020 ont été arrêtés par le onseil d’ dministration selon le principe de continuité d’exploitation au vu des prévisions d’activité et de trésorerie.
Prochain rendez-vous :
Assemblée Générale des actionnaires : le 27 mai 2021

